|
|
| ขณะนี้คุณกำลังอยู่ที่ เคมีออนไลน์/สารและการเปลี่ยนแปลง | => การจัดจำแนกสาร 3 |
| Page selector : หัวข้อก่อนหน้า 0 1 2 4 5 6 7 หัวข้อถัดไป | |
|
- สารบริสุทธิ์ - |
| .......สารบริสุทธิ์ คือ สารที่ประกอบด้วยสารเพียงชนิดเดียว อาจเป็น ของแข็ง ของเหลว หรือ ก๊าซ ก็ได้ เช่น เหล็ก ทองแดง น้ำ น้ำตาล ซึ่งยังแบ่งย่อยได้เป็นธาตุและสารประกอบ | |
|
|
|
1. จุดเดือด จุดหลอมเหลว
คงที่
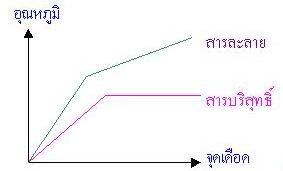  +ข้อสังเกต+
สารละลายจะมีจุดเดือดสูงกว่าสารบริสุทธิ์ แต่มีจุดหลอมเหลวต่ำกว่าสารบริสุทธิ์ ยกเว้น! สารละลายพวก Azeotropic หรือสารละลายที่ระเหยง่ายและแตกตัวเป็นไอออนได้ แต่ถ้าเป็นสารไม่บริสุทธิ์อื่นๆ จุดเดือดจะไม่คงที่แต่ระบุ กราฟแน่ชัดไม่ได้ |
|
|
|
|
|
2. สารบริสุทธิ์จะมีจุดเยือกแข็งคงที่
|
|
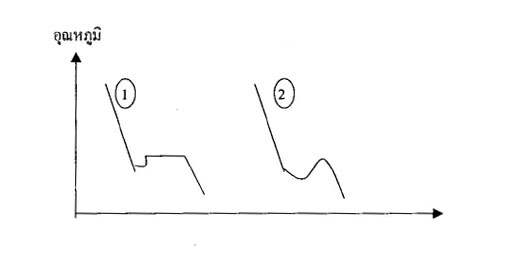 จากภาพ จะพบได้ว่า หมายเลข 1 คือสารบริสุทธิ์ เนื่องจากมีจุดเยือกแข็งคงที่ หมายเลข 2 คือสารไม่บริสุทธิ์ เนื่องจากมีจุดเยือกแข็งไม่คงที่ |
|
|
|
|
|
3.ช่วงการหลอมเหลวแคบ
|
|
|
ช่วงการหลอมเหลวคืออะไร? ตัวอย่างเช่น... |
|
| หมายเหตุ : แต่ละที่จะกำหนดช่วงการหลอมเหลวแคบกว้างไม่เท่ากัน เราจึงไม่ต้องจำว่าช่วงการหลอมเหลวเท่าใดแคบ เท่าใดกว้างโจทย์จะกำหนดมาให้เลย (แต่ส่วนมากจะไม่เกิน2๐C ) | |
|
|
|
|
: คำอธิบายเพิ่มเติม
:
|
|
|
|
......ที่สารไม่บริสุทธิ์มีจุดเดือดไม่คงที่เนื่องจากสารละลายประกอบด้วยสารหลายชนิด เมื่อถึงจุดเดือดของสารชนิดหนึ่ง สารนั้นจะระเหยไป เหลือแต่สารอื่นซึ่งมีจุดเดือดต่างออกไป จึงทำให้สารไม่บริสุทธิ์มีจุดเดือดไม่คงที่ |
|
|
: ตัวอย่างเสริม : |
|
|
จงสรุปข้อมูลจากกราฟด้านล่าง
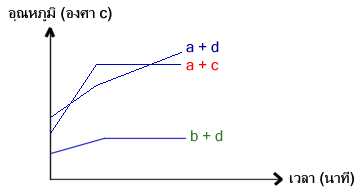 |
|
|
|
|
|
| ขณะนี้คุณกำลังอยู่ที่ เคมีออนไลน์/สารและการเปลี่ยนแปลง | => การจัดจำแนกสาร 3 |
| Page selector : หัวข้อก่อนหน้า 0 1 2 4 5 6 7 หัวข้อถัดไป |